溶血尿毒癥綜合征 溶血-尿毒癥綜合征溶血尿毒癥綜合癥溶血
溶血尿毒癥綜合征 溶血-尿毒癥綜合征溶血尿毒癥綜合癥溶血百科
Gasser(1955)首先報道5例兒童發生溶血性貧血,急性腎功能不全和血小板減少等綜合表現.以後對這種具有三聯綜合征者稱為溶血尿毒癥綜合征(haemolyticuraemicsyndrome,HUS),也有人稱其為微血管病性溶血性貧血(microangiopathichemolyticanemia).典型的HUS系一種伴有紅細胞形態異常,臨床以溶血性貧血、血小板減少、急性腎衰竭為特征的綜合征.血管內皮損傷致腎內微血管性溶血及血管內凝血血管內皮損傷是所有HUS發病機制的中心環節,也是始動環節,內皮細胞損傷可通過炎癥和非炎癥兩條途徑,STEC來源的脂多糖(LPS)可激活白細胞,激活中性粒細胞釋放TNFα,IL-1,內彈力酶及氧自由基,刺激細胞因子TNFα,IL-1的合成,LPS和細胞因子具有協同作用,可損傷內皮細胞,TNFα或LPS均可刺激接觸Stx的內皮細胞凋亡,引起血管內皮細胞損傷,各種原因所致腎臟毛細血管內皮細胞的損傷,引起纖維蛋白沉積,內皮細胞損傷表現為細胞腫脹,脫落,內皮細胞損傷後,基底膜暴露,激活血小板和導致局部血管內血栓形成,一方面因為紅細胞及血小板受到機械性損傷,造成微血管病性溶血性貧血和血小板減少,另一方面由於微血管病和內皮細胞的腫脹,在受損部位血小板黏附,聚集,形成血栓,引起腎內微血管的血栓栓塞,導致腎小球濾過率急劇下降,重癥可發生腎皮質壞死,最終發生急性腎功能衰竭.
溶血尿毒癥綜合征 溶血-尿毒癥綜合征溶血尿毒癥綜合癥溶血
溶血尿毒癥綜合征 溶血-尿毒癥綜合征溶血尿毒癥綜合癥溶血病因
遺傳因素(20%):
HUS通過常染色體隱性或常染色體顯性遺傳方式遺傳,常染色體隱性遺傳在同一傢族的兄弟姐妹間發病間期可達1年以上,兒童受累機會高於新生兒及成人,預後較差,死亡率接近65%,大多數常染色體顯性遺傳HUS患者為成人發病,可反復發作,預後較差.
感染(20%):
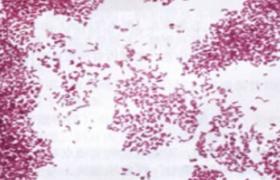
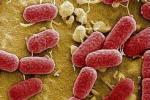
(1)細菌:分泌Shiga毒素的大腸埃希桿菌感染,導致Shiga毒素相關性HUS(Shigatoxinas-sociatedHUS,StxHUS)占75%,是最常見的類型,分泌Stx的大腸埃希桿菌(STEC)可分泌Stx1,Stx2及其衍生物,志賀痢疾桿菌,沙門菌,假單胞菌屬感染也與HUS發病有關,肺炎鏈球菌等細菌能使紅細胞表面的T-F抗原與自身的T-F抗體反應,造成血細胞凝集而誘發HUS.
(2)病毒:現已分離出多種可能與本病相關的病毒,某些病毒感染後HUS的發病率高,常見者為柯薩奇病毒,ECHO病毒,流感病毒,EB病毒,黏液病毒,蟲媒病毒,水痘病毒,傳染性單核細胞增多癥病毒等.
(3)其他:立克次體和支原體感染與HUS有關也有報道.
癌癥伴隨HUS(15%):
某些腫瘤如胃癌,前列腺癌,在用絲裂黴素C治療腺癌時尤易發生,發生率為4%,一般用藥6~12個月後發病,常伴有急性呼吸窘迫綜合征,預後差,病死率高達70%,此外,長春堿,順鉑,博來黴素,5-氟尿嘧啶,爭光黴素等均可誘發HUS.
藥物或某些化學物質(15%):
除一些抗腫瘤藥物外,避孕藥或其他含雌激素的藥物,青黴素,氨芐西林,免疫抑制劑,環孢素,奎寧,可卡因等可誘發HUS,食用瞭變質的食物,食物內某種毒素可直接或間接造成內皮細胞損傷.
其他因素(10%):
成人HUS也常見於急進性高血壓,風濕性疾病,骨髓移植或腎移植後,內分泌代謝異常如前列環素不足,α-生育酚不足,維生素B12代謝異常等均可為本病的誘發因素.
發病機制
1.血管內皮損傷致腎內微血管性溶血及血管內凝血血管內皮損傷是所有HUS發病機制的中心環節,也是始動環節,內皮細胞損傷可通過炎癥和非炎癥兩條途徑,STEC來源的脂多糖(LPS)可激活白細胞,激活中性粒細胞釋放TNFα,IL-1,內彈力酶及氧自由基,刺激細胞因子TNFα,IL-1的合成,LPS和細胞因子具有協同作用,可損傷內皮細胞,TNFα或LPS均可刺激接觸Stx的內皮細胞凋亡,引起血管內皮細胞損傷,各種原因所致腎臟毛細血管內皮細胞的損傷,引起纖維蛋白沉積,內皮細胞損傷表現為細胞腫脹,脫落,內皮細胞損傷後,基底膜暴露,激活血小板和導致局部血管內血栓形成,一方面因為紅細胞及血小板受到機械性損傷,造成微血管病性溶血性貧血和血小板減少,另一方面由於微血管病和內皮細胞的腫脹,在受損部位血小板黏附,聚集,形成血栓,引起腎內微血管的血栓栓塞,導致腎小球濾過率急劇下降,重癥可發生腎皮質壞死,最終發生急性腎功能衰竭.
2.Stx對腎小管上皮細胞的損傷作用產生Stx的大腸埃希桿菌感染後,Stx進入血循環,與腎內皮細胞糖脂受體糖鞘脂受體結合,抑制內皮細胞蛋白合成,引起細胞壞死或凋亡,急性小管間質損傷可導致急性腎功能衰竭.
3.細菌毒素與神經氨酸酶直接損傷上皮細胞細菌內毒素可使細胞因子釋放介導內皮細胞損傷,激活巨噬細胞使活性氧化代謝產物增加,激活中性粒細胞,增加細胞表面受體表達,促進白細胞聚集,致中性粒細胞介導的細胞損傷,此外還能激活補體與血小板活化因子而參與發病.
神經氨酸酶為一種有害因子,可損傷腎小球毛細血管內皮細胞而致病,肺炎雙球菌也能產生此酶.
4.血凝及纖溶異常HUS時血栓素(TXA2)與血小板活化因子(PAF)等和前列環素(PGI2)之間的平衡遭破壞,HUS時受損的血管內皮細胞不能產生PGI2,內皮細胞產生PGI2的促進因子亦減少,PGI2降解加速,消耗增加,PGI2減少使血小板聚積,粘連作用加強,有利於血小板在受損的腎小球毛細血管壁沉積而發病,腎臟產生的PAF可促使血小板持續活化和血小板在腎小球毛細血管內沉積,促使血小板聚集與形成血栓,導致腎功能急劇惡化,血管內皮產生的纖維蛋白溶酶原活化因子減少,也容易形成血栓,血管內皮產生的巨大分子血管性血友病因子(VWF)多聚體促進血小板與受傷的血管壁黏附,促進血栓形成.
近來經研究認為下述因素最終導致凝血功能亢進,血小板黏附和聚集功能增強,而纖溶活性低下:
(1)炎癥介質:特別是TNFα,IL-6,IL-8,參與內皮細胞損傷及活化.
(2)血小板及凝血過程的激活.
(3)內皮細胞PGI產生減少.
(4)內皮細胞內皮素-內皮舒張因子失平衡.
(5)脂質過氧化物.
(6)循環免疫復合物及抗內皮細胞抗體.
5.免疫機制HUS的發病可能與免疫有關,HUS發病前大部分病例有呼吸道或胃腸道感染,符合抗原-抗體反應的發病過程,部分患者於發病初期有IgA,IgM升高,C3下降,腎組織免疫熒光檢查可見IgM,C3,C1q,備解素及纖維蛋白原的沉積.
6.妊娠易致HUS的機制孕婦血循環中的纖維蛋白原,第Ⅴ,Ⅶ,Ⅷ凝血因子均有不同程度的升高,同時纖溶能力降低,妊娠的某些合並癥(流產,胎盤早剝,子癇等)由於胎盤釋放出的凝血致活酶(thromboplastin)可導致凝血機制活化,更易促發孕婦在原有的高凝狀態下血管內凝血,在腎內形成微血栓而致病.
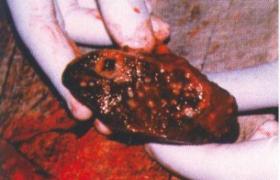
7.病理嚴重受累的腎小球有充血,梗死,毛細血管內可見透明血栓,病變較輕者,毛細血管壁增厚,有嗜酸性,糖原染色呈弱陽性的透明物質沉積在內皮細胞與基底膜之間,系膜細胞增生也較明顯,電子顯微鏡下,內皮細胞損傷主要見於腎小球毛細血管和腎小動脈,顆粒狀或纖維狀電子致密物存在於內皮細胞及其與基底膜間的空隙,腎小球毛細血管內有大量血小板,毛細血管,內皮下和系膜有纖維素沉積.
受累的入球小動脈和葉間動脈壁發生纖維素樣壞死,可以見到內皮細胞的剝離,血栓內的纖維蛋白間的腔隙較腎小球毛細血管內形成的腔隙大,有小的動脈瘤形成,尤其在入球小動脈,腎皮質壞死可呈灶性,或累及全部.
溶血尿毒癥綜合征 溶血-尿毒癥綜合征溶血尿毒癥綜合癥溶血
溶血尿毒癥綜合征 溶血-尿毒癥綜合征溶血尿毒癥綜合癥溶血症状
HUS在任何年齡均可罹病,但主要發生在幼兒及兒童,性別無明顯差異,但成人以女性為多,可能與妊娠易發生HUS有關,農村較城市多見,通常呈散發性,一年四季均有發病,但以晚春及初夏為高峰,病情輕重不一,且有不同的變異性.
1.前驅癥狀典型者有前驅癥狀,以胃腸癥狀為主要表現,如食欲不振,嘔吐,腹瀉,腹痛,伴中等度發熱,少數有嚴重血便,1/3小兒有上呼吸道感染癥狀,此期一般1~7天,然後經過1~5天無癥狀期進入急性期.
2.急性期表現急性期典型所見是溶血性貧血,血小板減少和急性腎功能衰竭.
(1)溶血性貧血:溶血性貧血表現為短期內血色素明顯減少,貧血的程度與急性腎衰的嚴重程度不一致,小兒表現為面色蒼白,黃疸一般不明顯,或僅面部呈檸檬黃色,病初2周內可屢有溶血危象發作,於數小時內血紅蛋白即可下降30~50g/L,檢查末梢血象白細胞及網織紅細胞增高,血塗片可見異形紅細胞及紅細胞碎片,紅細胞可呈三角形,盔甲型,芒刺型,血非結合膽紅素升高,紅細胞壽命縮短,平均為3天,貧血持續1~3周後逐漸恢復.
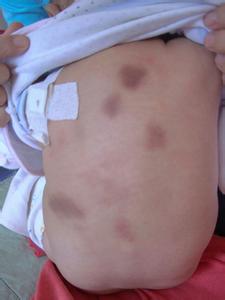
(2)血小板減少:90%患者有血小板減少,主要由於外周破壞增加所致,血小板存活時間由正常的7~10天縮短為1.5~5天,血小板減少一般持續7~14天,少數恢復較慢,由於血小板減少而有出血傾向,表現為鼻出血,牙齦出血,皮膚瘀點或小血腫,嘔血,便血,咯血,眼底出血,甚至腦出血.
(3)急性腎功能衰竭:腎損害導致輕重不一的急性腎功能衰竭,輕者僅暫時性尿量減少,輕度腎功能減退,有時稱為實驗室性溶血尿毒綜合征,重者呈少尿型,少尿可持續2天~8周,尿檢查有蛋白,紅,白細胞及管型,與此同時出現其他急性腎衰的癥狀,如氮質血癥,高鉀血癥,代謝性酸中毒,高血容量,高血壓等,由於溶血大量紅細胞破壞釋出尿酸,故易出現高尿酸血癥,一部分病例由於嚴重貧血,少尿,高血壓,電解質紊亂等而誘發充血性心力衰竭,心律失常,心跳驟停而致死,HUS慢性腎功能衰竭的發生率為10%~40%,需長期透析治療以維持生命.
(4)神經系統癥狀:HUS可累及中樞神經系統,部分患者有程度不一的神經精神癥狀,如頭痛,嗜睡,易激惹,肌震顫,驚厥,甚至昏迷,部分病例遺留神經系統後遺癥,如行為異常,學習困難,嚴重智力減退,甚至癲癇發作.
(5)其他表現:侵犯心臟者由於心肌內微血管血栓導致心肌壞死,引起心力衰竭,心律失常,重者發生猝死,肺內微血管血栓可導致胸悶,咯血,肺功能不全等表現.
3.變異型HUS
(1)傢族性HUS:傢族性病例發病除遺傳因素外,可能共同遭受環境中致病因子而發病.
(2)復發或反復性HUS:復發時很少有典型的前驅癥狀,成年婦女的復發常發生在孕期,病死率高達30%.
(3)產後型HUS:多有流感樣征群,吐瀉,或尿路感染等癥狀,病情重者預後差.
傳統的HUS診斷主要依據臨床,即存在微血管性溶血性貧血,血小板減少及腎臟損害(血尿,蛋白尿及腎功能不全)即可診斷為HUS,但事實上臨床所見HUS變化多,表現不一,文獻報道許多HUS的臨床表現不典型,如貧血及血小板減少可很輕微甚至不出現,也可無腎臟病變臨床表現,因此,對HUS的診斷應從HUS的基本病理改變及病理生理角度去認識,而出現腎臟病改變對HUS的診斷具有決定性的作用.
溶血尿毒癥綜合征 溶血-尿毒癥綜合征溶血尿毒癥綜合癥溶血
溶血尿毒癥綜合征 溶血-尿毒癥綜合征溶血尿毒癥綜合癥溶血检查
1.嚴重的溶血性貧血在數天~數周內可發生反復的溶血,網織紅細胞增加,髓母紅細胞增加,親血色蛋白減少.
2.Coombs試驗多為陰性,紅細胞酶活性正常.
3.末梢血塗片可見到怪異形狀紅細胞,盔形細胞和破碎的紅細胞.
4.血小板減少常見,持續數天至數周.
5.其他
(1)凝血酶原時間:部分患者凝血活酶時間正常或輕度縮短,Ⅴ,Ⅷ因子正常或稍增加;纖維蛋白裂解產物增加,ATⅢ可減少.
(2)血清C3,C4和CH50可下降:C3可沉積在某些病人的腎小球內;血清IgG濃度開始下降,而IgA和IgM增加;在腎小球系膜區常檢出IgM沉積物,纖維蛋白原沉積常見.
(3)尿液檢查:可見蛋白尿,血尿和管型尿和BUN增加.
(4)電解質紊亂,包括血清鈉,碳酸氫鹽和鈣下降,血鉀可高或低,血清膽固醇,三酸甘油酯和磷可增加.
1.腎組織學檢查HUS的基本病理改變是血栓性微血管病變,腎臟是HUS的主要受累器官,腎組織學檢查可見腎臟呈微血管病變,可累及腎小球及腎間質動脈,腎小球主要病變表現為內皮細胞腫脹,內皮下間隙擴大導致毛細血管壁增厚,管腔變窄,在內皮下可見纖維蛋白及脂質沉積,毛細血管腔內可見紅細胞,血小板及微血栓,系膜區增寬,系膜細胞溶解或呈泡沫樣細胞,部分病例可出現新月體及襻壞死,嚴重者小動脈受累,腎皮質壞死,病變腎小球可呈灶性分佈,此外腎小球可表現有缺血征象,腎小球GBM增厚,皺縮,腎小球襻塌陷,包囊增厚,腎間質微動脈及小動脈內皮細胞增生,內膜腫脹,管壁壞死,管腔變窄,有些腔內可見血栓,腎小管,間質病變常為中,重度,有的出現腎小管壞死,病程晚期可見小動脈纖維增生,最終導致腎小動脈及腎小球硬化,玻璃樣變,腎小球荒廢,腎小管萎縮及間質纖維化.
免疫熒光檢查,絕大多數微血栓內可見纖維蛋白,動脈壁上可有IgM,C3,C1q及備解素沉積,電鏡示腎小球腫脹的內皮細胞可從GBM剝脫,沿內皮細胞側可見新形成的薄層基底膜,內皮下存在細胞顆粒狀電子疏松物質,毛細血管腔變窄,可見含脂肪滴的泡沫細胞,系膜基質水腫,甚至溶解.
腎小球及動脈受損的程度及范圍可因不同的病因,病情,病期及發病年齡而各異,有學者將HUS的腎臟病變分為3種類型:
(1)腎小球損傷為主.
(2)血管損傷為主.
(3)腎皮質壞死.
這三種病變也可互相重疊,在同一病例,腎小球病變可與嚴重動脈病變同時存在,兒童患者病變以腎小球為主,血管病變輕微,偶可見內皮下間隙增寬,成人HUS動脈病變較明顯,因此預後不如兒童.
HUS除腎受累外,還可累及中樞神經系統,胃腸道,肺,心臟及其他器官,也會發生微血管栓塞及壞死性病變.
2.常規B超,X線,CT等檢查.
溶血尿毒癥綜合征 溶血-尿毒癥綜合征溶血尿毒癥綜合癥溶血预防
本病為多病因引發的疾病,對遺傳因素所致的HUS無有效預防措施,對其它原因引發本病者,要積極治療原發病,或避免腎毒性藥物的應用,以預防HUS的發生和進行性加重.